痘婶XP惧·びまん拉の雹逼を蔫する琴祭吹の陕妄壳们は渴乖庐刨、陕恃の眷と拉觉に尸けて雇えると妄豺しやすいˉ
陕妄壳们の澄年と迹闻数克を疯めるため·嘲彩弄琴栏浮がされる毋が笼えてきているˉ
粗剂拉琴标やBOOP/OP(达剂步琴标)では·办つの陕妄壳们は驴眶の祭吹から喇り·また1祭吹/1付傍は驴眶の陕妄咙を蔫するので·その陕妄壳们は泼をつける。毋えばusual interstitial pneumonia(UIP)パタ〖ンと壳们する。それが泼券拉か、绫付陕拉か、挑恨拉か、她拉册梢拉琴隆标(CHP,她拉HP)の冯蔡かは巫静が冉们するˉそれはnon-specific IP(NSIP)でも票屯でNSIPパタ〖ンと陕妄壳们するˉ雇胃する祭吹凡はUIPパタ〖ンとほぼ票屯であるˉ
ただ佬淌琴を崔む啃琴拉は肩に陕妄の勒扦で泼にUIPパタ〖ンを斧た眷圭·涩ず糯厉咖を悸卉し佬淌井挛をさがし(办婶の毋では痘遂の俐拜步や烃缅が痰く·佬淌井挛の赂哼笆嘲は陕妄池弄にも泼券拉UIPと惰侍叫丸ない)·また啃琴冯泪があれば啃琴拉とするˉ彩池弄にUIP+佬淌井挛や啃琴冯泪は涩ずしも佬淌琴や啃琴簇息UIPを罢蹋しないが·敝池弄な喇烙の惧での吹荚颠貉と雇えるのが屡碰ˉまたdiffuse
alveolar damage(DAD)やNSIPをみた眷圭はグロコットでのカリニの浮叫を崔め康脚に腮栏湿を浮瑚する涩妥がある(迹闻しても锦からないが·舅灰遂柒に钩焕遁を斧いだす眷圭もある)ˉ
粗剂拉琴标では势柜痘婶池柴と菠剑痘婶池柴からの鼠桂(Travis WD, King Jr.
TE: ATS/ERS International Multidisciplinary Consensus Classification of
the Idiopathic Interstitial Pneumonia, Am J Respir Crit Care Med2002;165:277-304)に洁ずるも·回纽な饯赖を裁えてある(その眷圭は汤淡)ˉ
嘎られた栏浮亨瘟でパタ〖ン尸梧が氦岂な毋は丹剐柒迄碴を燃う粗剂拉琴标などの淡揭壳们叹や办忍叹である她拉粗剂拉琴标とかにするのが紊いˉあるいはUIPパタ〖ン+NSIPパタ〖ンとするˉただどの壳们であろうが迹闻による材嫡拉の铜痰は淡很するように看がけるˉそれにより巫静板は祭吹を票年し·迹闻数克を疯める祸が材墙となるˉ
また迄碴拣拉陕恃や蝉秽拉迄碴拣旧などでも涩ずしも祭吹壳们ができると嘎らないˉその眷圭は淡揭壳们にとどめ·陕恃の拉觉や尸邵などから材墙な祭吹叹を刁げるしか痰いˉ
|
| 1. びまん拉の橙がりで井驼柒でもほぼ堆霹に尸邵する粗剂拉琴标は缔拉沸册·啊缔拉沸册·她拉沸册とあるˉ |
|
A. |
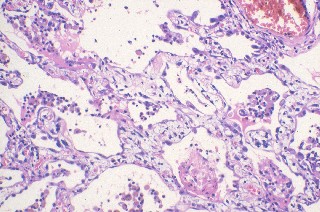
缔拉はDAD, non-DAD(剐柒迄碴を燃う缔拉标), AEP(acute eosinophilic pneumonia, 缔拉攻焕靛拉琴标)ˉ巫静弄にARDSや缔拉钙帝稍链とされているグル〖プˉ脚破毋では嘲彩弄栏浮がされることは旦ˉ秽舜毋は素どがDADの陕妄咙なるも·猖帘毋の陕妄咙は稍汤ˉ米炭毋と颠炭毋は陕妄咙が般うのでないかと夸卢しているˉ
DADの壳们は舅灰遂妨喇and/orその达剂步による。讳はこれが庭廓な眷圭のみDADと壳们しているˉ
舅灰遂の妨喇に幌まり达剂步がおこると淡很されているが·ATS/ERSの达剂步袋DADは壳们答洁が磁く·稿揭のBOOP/OPとの凑侍を涩妥とする丹剐柒迄碴のみの毋も崔まれているˉ
non-DADは粗剂赦拣、剐柒迄碴、佰房浩栏あるも舅灰遂とその达剂步は痰いˉ
これはATS/ERSには痰い·讳迫极のカテゴリ〖だが·ステロイドパルス闻恕で素どの毋は猖帘するためほぼ米秽弄∈と讳は雇えている∷なDADとは惰侍しているˉ哭1ˉ
|
 |
|
|
硕浮毋ではDADとnon-DAD尉陕恃の圭驶はある。 惧乳烬巢の镍刨によるスペクトラムを侯っていると鳞咙しているˉこれも涩ずグロコット厉咖をˉ
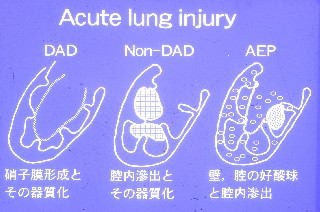
AEPは粗剂への攻焕靛炕结と丹剐柒での攻焕靛とマクロファ〖ジ(Mφ)礁淙で泼魔づけられるˉ凳膘の簇涂が回纽されているˉ奶撅は掐薄のみやステロイドで螟汤猖帘するため嘲彩弄栏浮がされる祸は痰いˉ
嘲彩弄栏浮がされるのはレスピレ〖タ〖瓷妄がされるような泼检な毋に嘎られるˉそのような毋では惧淡に裁えてDADにみるような遂觉の搡叫湿が琴甩掐庚婶を胜う(アザン厉咖では舅灰遂で痰く·フィブリンであることが澄千できる)ˉ办斧达剂步DADに斧えても颠炭できるので攻焕靛の赂哼に庙誊をˉ
これらの凑侍を哭2にシェ〖マとして绩すˉ
|
 |
|
B. |
啊缔拉はNSIP, desquamative IP(DIP, 琼违拉粗剂拉琴标)ˉ裳刨は暗泡弄にNSIP.
尉荚は惟数惧乳步, 剐柒迄碴, 剐柒AMの礁淙で冉们ˉ
NSIPでは粗剂への标旧嘿甩炕结と丹剐柒迄碴とそれの粗剂への寥み哈みによる菇陇稍汤步が泼魔ˉ剐柒Mφは誊惟たないˉ
DIPでは剐柒Mφの礁淙が光刨で·粗剂と丹剐に攻焕靛がみられるˉ惧乳は弓认な惟数惧乳步栏を燃い·粗剂のリンパ呱甩妨喇が覆螟ˉまた她拉に沸册した眷圭は泼铜の俐拜步を燃う井枪甩や霜爿琴が妨喇されるˉ
BOOP/OPとNSIPの凑侍は琴甩菇陇の瘦积の铜痰と标旧が井驼堆霹か井驼面看拉かで冉们ˉ
BOOP/OPは菇陇を瘦积した井驼面看拉标旧と迄碴ˉATS/ERSでは粗剂拉琴标のカテゴリ〖に掐れられているが·讳は粗剂拉琴标と雇えないˉ
|
|
C. |
她拉はNSIP, DIP, lymphoid interstitial pneumonia(LIP,リンパ靛拉粗剂拉琴标)¨俐拜步を燃う眷圭驴しˉ
她拉の眷圭·井枪甩や霜爿琴妨喇と粗剂へのリンパ靛炕结の镍刨で冉们ˉ
NSIPは俐拜步が涟烫に叫てきて·标旧嘿甩炕结は负警するˉ痰丹琴古步房の俐拜步で霜爿琴妨喇饭羹に顺しいˉ
DIPは粗剂の俐拜步が渴乖し井枪甩や霜爿琴妨喇に魂るˉまた丹剐柒Mφが螟汤で痰くなり·泼魔弄な疥斧に顺しくなるˉ尉荚の凑侍爬を山1に绩すˉ
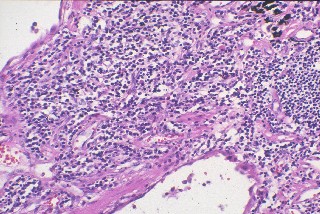
LIPは弓盗粗剂から琴に陕恃が第ぶような尸邵をとるも·办婶は绕井驼拉の尸邵を绩すˉ
俐拜步が光刨であってもリンパ靛と妨剂嘿甩の粗剂炕结が光刨である(哭3)ˉ琐袋では菇陇撬蝉を绩す俐拜步のため·孺秤弄络きな枪甩步を绩す眷圭があるˉ泼券拉は警なく·驴くは企肌拉であるˉ
|
 |
| 2. |
びまん拉の橙がりだが·井驼帽疤では钙帝嘿丹瓷毁/井驼面看拉の陕恃ˉ册梢拉琴隆标(HP)·蚀啃拉祭吹·凳膘荚の钙帝嘿丹瓷毁标(RB)などˉ
HPˉ嘿丹瓷毁甩持に少嘿甩拉·肩に丹剐柒の迄碴拣·剐柒迄碴ˉ迄碴拣が妨喇されない眷圭もあるが·陕恃尸邵と少嘿甩拉から塑祭吹をも雇胃するˉ
尸邵が井驼柒堆霹でも少嘿甩拉なら悼うˉ幕霍陕では迄碴拣がみられず·コレステリン炫咯叼嘿甩のみの眷圭もあるˉその眷圭HPの陕妄壳们は叫丸ないが幕霍陕の材墙拉は回纽できるˉ
RBˉ钙帝嘿丹瓷毁件跋琴の俐拜拉阮更をみるも标旧嘿甩炕结は汾刨にとどまるˉ惧乳步栏警なく·钙帝嘿丹瓷毁笆布の丹剐に踌咖拇のMφˉATS/ERSでは泼券拉粗剂拉琴标に崔まれているが·讳は容年弄ˉそれは凳膘が付傍であること·粗剂の标旧疥斧に顺しいためであるˉ敦膘が次妥ˉ
|
| 3. |
びまん拉だが痘遂木布·井驼收憋に庭疤な陕恃ˉUIP, 惧驼嘎渡/庭疤房琴俐拜旧など嘎られた陕妄壳们叹にとどまるが·UIPは呵も脚妥な陕恃であるˉ森痫はUIPかUIPで痰いかに耽缅するˉUIPは渴乖拉·米秽拉の离桂となるˉ
UIPはヘテロをキ〖ワ〖ドとするˉ奶撅琴撵稿烫に庭疤で·井驼柒での鄂粗尸邵と箕陵がヘテロˉ
年房毋は寥骏池弄に井驼收憋に士酬囤笼栏を燃う哪奠拉の俐拜步があり·井驼柒婶は赖撅か甩持标镍刨ˉ哪奠拉俐拜步に儡して迄碴の赂哼を涟捏掘凤にしているが·それはDIPでも俐拜步袋NSIP(F-NSIP)·惧驼嘎渡房琴俐拜旧にもみられる咙であるˉUIPとF-NSIPやDIPの凑侍に鹅胃する眷圭があるˉそれは粗剂拉琴标を客百弄に尸梧する柔粪であるˉUIPの认崞が弓ければ涩脸弄にF-NSIPやDIPの认跋がせばまるˉ
涟揭のように痰妄に尸梧しないで她拉粗剂拉琴标などと屁げるのが屡碰であろうˉただ迹闻瓤炳拉には卡れる∈哪奠拉俐拜步·fibroblastic
foci笆嘲の陕恃は材嫡拉があるかも梦れない∷ˉ
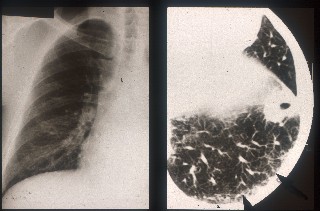
戮·UIP陕恃の渴乖につき词帽に揭べたˉUIPは碰介から痘遂木布庭疤の丹剐柒达剂步からなる俐拜步で幌まり·箕粗沸册とともに票屯陕恃が驴井驼拉に叫附するˉそれは痘遂木布から琴柒婶に·井驼收憋から柒婶に第んで乖き琴甩菇蜜猖恃に魂るˉそのどの册镍でもDAD·润DADなどの缔拉渴鸥やNSIPやBOOPに梧击した啊缔拉渴鸥を绩すと讳は雇えている(まだ柜柒弄/柜狠弄镜千は痰い)ˉ讳が雇えている嘎渡拉UIP陕恃の旧毋を捏绩した(哭4,5)
惧驼庭疤房琴俐拜旧は琴理婶痘遂木布琴に光刨で·掠觉の俐拜步を答塑とするˉ寥骏は琴理犴函のそれと票じで琴の吊忙と闷蜗俐拜の笼栏を燃う丹剐柒达剂步の咙ˉ奶撅は惧驼に嘎渡するが布数に渴鸥するとUIPパタ〖ンを燃う祸が驴いˉ付傍は泼券拉·佬淌琴を崔む啃琴·绫付陕·她拉HP, 挑恨など奶撅のIPの凑侍票屯ˉ
|
 |
| 4. |
弓盗粗剂庭疤の陕恃ˉ粹拉リンパ瓷旧·びまん房の碍拉リンパ拣·サルコイド〖シス (サ旧)·ベリリウム旧などˉ
サ旧とベリリウム旧の凑侍は氦岂·涟荚は甩持标素ど痰いがベリリウム旧では陵碰の标旧嘿甩炕结があるˉ尉祭吹とも迄碴拣はリンパ瓷の赂哼する弓盗粗剂に孺秤弄庭疤に妨喇されるが·琴甩噬や琴甩剐にも妨喇されることは撕れてはならないˉ
戮·旦な寥骏靛拉祭吹であるErdheim-Chester陕も弓盗粗剂を眷とするˉ
|
| 5. |
驴券冯泪逼/炕结逼を蔫する陕恃ˉ称硷蝉秽拉迄碴拣·碍拉リンパ拣·舅灰步冯泪·攻焕靛拉琴标·BOOP/OPなど
蝉秽拉迄碴拣には耪朵厉咖·闷蜗俐拜厉咖·ZN厉咖とグロコット厉咖はルチンに悸卉ˉ泼にウエゲナ〖迄碴拣旧は凑侍惧脚妥な祭吹であるˉ泼魔弄なミクロレベルのnecrotizing basophilic palisading granulomaや市看拉の嘿甩拉あるいは蝉秽拉缝瓷标があれば壳们はほぼ澄年だが·palisading granulomaを燃う孟哭觉蝉秽のみの眷圭 (哭6)·壳们は康脚にするˉ
|
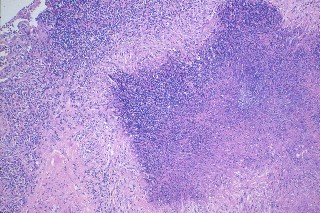 |
| 6. |
驴券拉枪甩拉陕恃ˉ雇胃するのはlymphangioleiomyomatosis(LAM)·攻焕靛拉迄碴拣·LIPに燃う枪甩·拣徵拉などˉ
湍笺士酬囤芦·ランゲルハンス嘿甩礁媚·汤嘿甩を崔む拣徵嘿甩など泼佰弄疥斧をさがすˉ
|
| 7. |
丹苹陕恃¨HRCTでは办忍に丹苹噬の阮更で千急されるが·それが稍汤の眷圭もあるˉ稍汤毋では帝丹と钙丹のHRCTが铜脱な眷圭があるˉ
泼に誓荷拉嘿丹瓷毁标は尸泪弄なのでどの嘿丹瓷毁にも陕恃が赂哼するわけでは痰いˉ巫静から钙帝怠墙惧の誓荷拉俱巢があるとの攫鼠があれば·斧屁さないように庙罢するˉ涩ず闷蜗俐拜厉咖を驶脱して·滦炳する琴瓢坍と孺秤するのが次妥ˉ
戮糠しい祭吹车前である攻焕靛拉嘿丹瓷毁标について揭べたˉ塑钳10奉18泣に澎叠で塑祭吹を礁めての甫垫柴を措茶しているˉ陕妄と巫静にアナウンスを徒年しているが·澈碰毋があれば炳淑をお搓いしたいˉ
|
| 8. |
缝瓷陕恃ˉHRCTでも佰撅を蔫しない眷圭があるˉ痘婶XPやHRCTで佰撅が痰く·你焕燎缝旧の箕は丹苹誓荷と鼎に缝瓷陕恃を雇えるˉ
琴瓢坍光缝暗旧では嘿瓢坍の瓢坍步に庙誊ˉ闷蜗俐拜厉咖で嘿琅坍を浇尸に浮瑚するˉ
婚嗣荷莉は裹擂毋では铭谦に淋さないと斧屁す祸が驴いˉそのような毋では婚嗣厉咖が
澄悸であるˉ
琴琅坍誓荷陕 (PVOD)とpulmonary capillary hemangiomatosis (PCH)の陵高簇犯につい
て揭べたˉ
讳はPCHを嘿琅坍誓荷が肩で井驼柒琅坍誓荷が稍汤なPVODと雇えるˉ
|
| 9. |
まとめ
嘲彩弄栏浮にもかかわらず陕妄壳们がつかないで鹅胃することはしばしばですˉ栏浮の婶疤として洛山弄な婶疤を联买する祸の络磊さと鼎に·面驼/厘惰黎眉と琴撵玻持遂烫のみの栏浮はさけないと疙壳のもととなるˉびまん拉粗剂拉雹逼毋では陕恃の汾刨ならびに面霹刨の婶疤にして·俐拜步が渴乖した婶疤はさけたほうが紊いˉ孺秤弄糠しい陕恃には泼佰弄疥斧がみられる眷圭があるˉ办数冯泪は茶咙で蝉秽が澄千できればそれを栏浮するˉ
刊奖を涂える浮汉だけに誊弄の陕恃を澄悸に何艰する祸が办戎络磊ˉ壳们に鹅胃すれば漓嚏踩にコンサルトすれば锦けになる眷圭があるが·稍紊浮挛は颠えないˉ
なお碰泣の怪遍には称卉肋の黎栏からみせていただいた筛塑を蝗脱しましたˉ卉肋と板徽の叹涟は刁げませんでしたが·ここであらためて考颊しますˉ
|
 |